Удк 546.212+547.45
Изучение разбавленных водных растворов
аминокислот методом светорассеяния.
Пешехонова
А.Л, Конторов А.М, Черников Ф.Р.
119991 Московский государственный
университет прикладной биотехнологии.
Исследовано
состояние воды в растворах аминокислот в концентрации 10-3-10-27
методом молекулярного флуктуационного светорассеяния.
Наблюдается несколько максимумов дисперсии от концентрации растворенного
вещества, в том числе в областях сверхмалых концентраций и мнимых растворов.
Полученные данные свидетельствуют о том, что в растворах происходит периодическая
смена определенных состояний воды.
Ключевые слова: вода, аминокислоты, лазерное
светорассеяния.
Studying the dilute solutions of aminoacids
with the method of dynamic laser light diffusion.
Key Words: water, aminoacids, dynamic light diffusion.
It has been researched
in the article that condition of water in the
solutions of aminoacids
( phenylalanine, alanin and treonin)
in concentration 10 3 - 1029 with the method of the molecular dynamic
light diffusion. Several maximal peaks
of dispersion are
supervised from the concentration of the dissolved substances including the
field of the superlow
concentrations and imaginary solutions.
The received facts that confirm that there is periodic charge of the
certain conditions of water in the
solutions.
В последние годы все больше ученых
обращаются к проблеме сверхмалых доз, расширился спектр биообъектов, на которых
проводятся эти исследования, возросло число химических веществ и физических
факторов, для которых обнаружена активность в сверхмалых дозах. Прежде всего нужно остановиться на понятии “сверхмалые дозы”. Так , Духович и соавт.
на основании данных о количестве клеточных рецепторов и сродства лигандов к ним
принимают за абсолютную границу
концентрацию 10-11 М. Для препаратов с низким сродством к рецепторам
сверхмалыми концентрациями можно считать и более высокие значения, в частности
, 10-9 -10-10. При таком классическом подходе,
даже в случае гипотетически более высокого, чем 10-12 М сродства лигандов к рецепторам, эта граница не может быть ниже 10-11
М. К близким выводам приходят исследователи, которые при определении
границы для СМД исходят из максимального сродства лигандов
к рецептору и поэтому считают СМД биологически активных веществ значения 10-13М
и ниже (1)
Существует
несколько теорий действия веществ в СМД. В их основе
лежат представления о концентрировании действующего вещества, о наличие высокоэффективных
систем усиления сигнала, о формировании ответа в условиях неравновесного
связывания лиганда с рецептором. Кроме того, было
предложено несколько авторских теорий. Так, Блюменфельдом
Л.А. была предложена релаксационная концепция биокаталитических
процессов, которая позволила предположить возможное объяснение действия СМД
биологически активных веществ на некоторые внутриклеточные процессы (2,3,4)
По мнению Ашмарина и др. (5-9) можно назвать, по крайней мере 4 системы, необходимые для реализации эффектов в СМД: каскадные
системы, амплифицирующие сигнал; собирательные, конвергентные
системы; накопители и транспортеры сигнальных молекул; супераффинные
рецепторы
Зайцевым С.В.
и др (10-12) предложена концепция адаптационного механизма
действия СМД, которая позволяет
объяснить все основные закономерности эффектов СМД с единой точки зрения.
Достаточно интересной теорией является теория Ямскова И.А (13-18)., который считает, что в основе действия
физико-химических факторов в механизме биологического эффекта СМД лежит
изменение пространственной организации микроокружения клетки –
микрогетерогенного геля, названного малым матриксом. Малый матрикс
микроокружения клетки обеспечивает восприятие, распространение сигнала по структуре
органа и затем уничтожение поступившего извне информационного сигнала. (19,20)
Однако
наиболее предпочтительной теорией действия веществ в СМД является “теория
водных кластеров и памяти воды”. Вода как химический объект является предметом
научных исследований вот уже на протяжении длительного периода времени и
интенсивность их не снижается и в настоящее время. Один из наиболее точных
научных подходов к изучению структуры воды предполагает исследование водных
кластеров в изолированном виде. Однако следует ожидать, что изолированные
водные кластеры при включении их в жидкую среду в большей степени модифицируются
вследствие сильно интерактивной природы молекул воды в жидком состоянии.
Заметим, что сведения об изолированных водных кластерах нельзя полностью переносить
на жидкое состояние. В высшей степени интересно было бы знать, можно ли изучать
водные кластеры в чистой воде. Но вряд ли это возможно, поскольку чистая вода очень
реакционноспособна. К тому же следует учитывать, что
состояние абсолютно чистой воды, подобно абсолютному нулю температуры
практически нельзя достичь.
Существует
другой подход к выявлению водных кластеров – изучение свойств очень
разбавленных водных растворов. Знание свойств разбавленных растворов важно
также для прикладного аспекта, хорошо известно множество областей их
применения. По исследованию очень разбавленных растворов выполнен значительный
объем работ, которые позволяют с большой вероятностью предполагать
существование в нормальных условиях стабильных водных кластеров, ответственных
за каталитические реакции, а также за стимуляцию разного рода биологической
активности (23-30)
В нашей работе для исследования были взяты растворы D и L-аминокислот
Материалы и методы.
Условия измерения: флуктуационный спектрометр АГЛС “Эдас-1”,регистрация
рассеянного света в режиме гомодинирования (смешение
пучков рассеянного на образце света от двух точек кюветы) под углом 90º,
наложение на образец постоянного магнитного поля напряженностью 280 А/м, предварительное освещение образца когерентным ИК-излучением сλ=890 нм,
накопление интенсивности рассеянного света в течение 3 мин с шагом интегрирования
5 мс.
По временным рядам
зарегистрированных значений интенсивности рассеянного света методом фурье-преобразования вычисляли спектральные характеристики:
спектральную плотность мощности и спектральную дисперсию в частотном диапазоне
0,35-0,5 Гц. Для полученных спектральных характеристик рассчитывали их
производные и интегралы.
Обсуждение и результаты.
На рис.1 представлены
кривые изменения интегральной дисперсии
растворов L-и D -фенилаланина, в
зависимости от концентрации. Здесь можно видеть наличие максимумов в области 10 -15 и 10-23 “мертвых зон” , что позволяет предположить наличие биологической активности
у данных аминокислот в сверхмалых дозах и в состоянии “мнимых растворов”
На рис. 2 представлены
кривые изменения интегральной дисперсии растворов L и D аланина. Тем
не менее и здесь видно наличие нескольких максимумов
на кривых, в том числе в области 10-9М
, 10-15 и 10-23 . Это позволяет с уверенностью
предположить наличие биологической активности и у этих веществ в сверхмалых
концентрациях.
На рис.3 представлены кривые изменения итегральной дисперсии растворов L и D-треонина . Видно наличие
нескольких максимумов активности на концентрационной кривой 10-11-10-25, 10-9
Таким образом, можно
предположить наличие биологической активности у L и D-фенилаланина треонина и аланина
Таким образом, с помощью
изучения свойств химических соединений методом динамического светорассеяния
можно предсказывать наличие у них биологической активности в сверхмалых дозах.
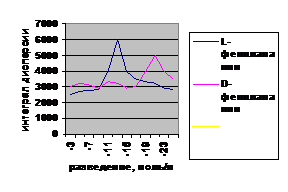
Диаграмма динамического светорассеяния фенилаланина измеренного на АГЛС “Эдас”.
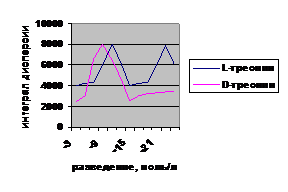
Диаграмма динамического светорассеяния треонина, измеренного на АГЛС “Эдас”.
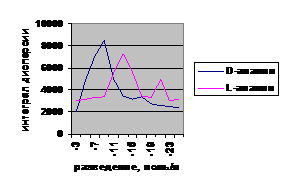
Диаграмма динамического светорассеяния аланина, измеренного на АГЛС “Эдас”.
Список литературы.
1.
Бурлакова Е.Б. Российский
химический журнал, №5, 1999
2.
Богатыренко Е.Н., Редкозубова Г.П., Конрадов А.А. и
др. Биофизика, 1989, т.34, с 327
3.
Блюменфельд Л.А. Биофизика,
1993, т.38, с129
4.
Блюменфельд Л.А. Российский
химический журнал, №5, 1999
5.
Сазанов Л.А., Зайцев С.Б. Биохимия, 1992,т.57, №10, с
1443
6.
Бурлакова Е.Б., Конрадов А.А., Худяков И.В., Изв.
АН СССР. Сер биол, 1990,№2, с184-193
7.
.Розен В.Б., Матарадзе Г.В.,
Смирнова О.В., Смирнов А.Н.. Половая дифференцировка функций печени. М.
Медицина, 1991, 336 с
8.
Rameshwar P., Ganea.D.,Gascon
P., J. Immunol.,1994., v 152.,#8,p 4044
9.
Coughlin S.R Proc. Nat. Acad
Sci
10.
Stock J., Borchuk., Chion F., Burchenal., J., Proc. 1999t.,Acad. Sci.
USA., 1985., v 82, p 8364-8368
11.
Koshland D., Biochemistry., 1998., v27,p. 5829
12.
С.И. Зайцев, А.М.Ефанов,
Л.А.Сазанов. Российский химический журнал, №5, 1999, с 28
13.
Ямсков И.А., Ямскова В.П. Росс. Химии.ж., 1998, т.42, №3, с 85-90
14.
Ямскова В.П., Ямсков И.А. Росс.
Хим. Ж., 1999, т.43, №2, с 74-79
15.
Бурлакова Е.Б. Вестн. РАН, 1994, т.64, №5, с 425-431
16.
Сазанов Л.А., Зайцев С.В., Биохимия, 1992, т.57,
вып.10, с 1443
17.
Бурлакова Е.Б., Конрадов А.А., Худяков И.В., Изв
АН. Сер биол, 1990, №2, с 184-193
18.
Блюменфельд Л.А Биофизика,
1993, №1, с 129-132
19.
Ф.С.Духович, Е.Н.Горбатова, В.Н.Курочкин,В.А.Петрунин. Росс. Хим. Ж., №5, 1999, с 12
20.
Зайцев С.В. А.М.Ефанов, Л.А.Сазанов Росс. Хим. Ж,,
№5, 1999, с 28
21.
Т.А.Воронина, Г.М.Молодавкин Росс. Хим. Ж. №5, 1999, с 89
22.
Т.И. Новожилова,
С.И.Малекин, В.К.Курочкин, С. Бугкала,
М.В.Киселевский Росс. Химич.
Ж., №5, 1999, с. 96
23.
Robinson,
Zhu S., Singh S., Evans M. Water in Biology. World Scientific. 1996
24.
Water.
A comprehensive treatise V 1-4. Ed Frank New-York: Plenum, 1972
25.
Debenedetti
P. Metastable Liquid, Conceps
and Prinsipal.
26.
Eisenberg
D., Kauzmann. The structure and properties of water.
27.
Stilinger F.H. Science, 1980, v 209,p 451
28.
Schindler
T., Berg C., Niedner-Schaterrburg G Chem. Phys.,
1995,v. 201.,p.491
29.
Lui K, Crusan J., Science, 1996,v 271 p.929
30.
Ш Ло, В.Ли Росс. Химич. Ж., №5, 1999, с 40
Поступила в редакцию
28 мая