Изучение влияния ацетилсалициловой и янтарной кислот на молекулярную структуру холестерина методом спиновой метки
Азонов Джахон Азонович,
доктор медицинских наук, профессор,
Джураев Хисори Шарифович,
кандидат химических наук,
Юсупов Изатулло Ходжаевич,
кандидат физико-математических наук,
Холова Шоира Алимахмадовна,
аспирант.
Государственный научно исследовательский институт питания.
Республики Таджикистан.
The influence of acetat and amber acids on the molecular structure of cholesterol by spin-echo method
D. A. Azonov, Kh. Sh. Juraev, I. Kh. Yusupov, Sh. A. Kholova.
State Scintific Research Institute of Nutrition of the Republic of Tajikistan.
Полученны результаты методом спиновых меток, свидетельствующие о том, что янтарная кислота и ацетилсалициловая кислота влияют на молекулярную структуру холестерина.
Ключевые слова: ацетилсалициловая кислота, янтарная кислота, холестерин, спиновая метка.
The evidence of the influence of acetate and amber acids on the molecular structure of cholesterol is shown.
Keywords: aspirin acid, succinct acid, cholesterol, spin labels.
Актуальность
Первые экспериментальные работы по применению метода спиновых меток в исследованиях биологических объектов и биополимеров были выполнены профессором Г.И. Лихтенштейном и его сотрудниками в Российской Федерации и в лаборатории Х. Мак–Коннела в США [1-3]. С тех пор этот метод нашел широкое применение в различных областях молекулярной биологии, биохимии, медицины, физической химии полимеров и т.д.
Суть метода заключается в том, что в макромолекулы исследуемого объекта вводят стабильный нитроксильный радикал, спектр ЭПР которого чувствителен к конформационной подвижности макромолекулы.
Целью исследования явилось изучение молекулярной структуры холестерина методом спиновых меток при погружении в ацетилсалициловую и янтарную кислоты.
Методы исследования
В настоящей работе приведены результаты влияние ацетилсалициловой (АЦК) и янтарной кислоты (ЯК) на подвижность спиновых меток, введенных в структуру холестерина (ХЛ). В качестве спиновых меток использовали нитроксильный радикал (НР) имеющий следующий структурную формулу:
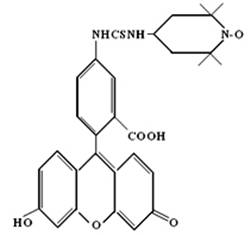
Навеску образца (холестерин) 25 мг помещали в пробирке, содержащей 1мл с этанолового (ЭТ) раствора спин – метки с концентрацией 4·10-3м. Смесь инкубировали в течение двух суток при комнатной температуре, затем добавили по 2 мг различных выше указанных органических кислот. Спектры ЭПР (первую гармонику сигнала поглощения) регистрировали на радиоспектрометре РЭ – 1306 в стандартных молибденовых ампулах с внутренним диаметром 3,0 мм в которые помещали по 25 мг спин – меченого образца. Спектры ЭПР образцов записывали при следующих условиях: затухание СВЧ мощности 5дБ; амплитуда развертки магнитного поля 200э, скорость развертки магнитного поля 40 э/мин; амплитуда ВЧ модуляции 0,3 Э [5] постоянная времени 0,1 с, частота модуляции 100 кГц.
Результаты и обсуждение
Результаты исследований влияния янтарной и ацетилсалициловой органических кислот на параметры спектров ЭПР спин-меченного холестерина представлены на рис. 1 и в таблице 1. Как видно (см. рис. 1) J0 – интенсивность центральной, J+1 – интенсивность низкопольной, J-1 – интенсивность высокопольной исследуемых систем резко отличаются друг от друга. Например, интенсивность системы 1) НР+ЭТ+ХЛ начало спектра 154 мм, а системы 2) НР+ЭТ+ХЛ+ЯК и 3) НР+ЭТ+ХЛ+АЦК соответственно конец спектра имеют значение 114 мм и 26 мм. Аналогичные изменения наблюдаются в значениях ΔHo, ΔH+1, ΔH-1 – ширина центральной, низкопольной и высокопольной компоненты спектров (см. табл. 1).
Таблица 1.
Параметры спектров ЭПР спиновой метки радикала (I) в среде этанола и модифицированного холестерина при погружении в янтарную и ацетилсалициловую кислоту.
|
№ |
Наименование вещества |
Спектральные параметры |
||||||||
|
J+1, мм |
J-1, мм |
J0 /J-1 |
J0, мм |
2A´z, Гс |
ΔH+1, Гс |
ΔH-1, Гс |
ΔH0, Гс |
τс сек. |
||
|
1 |
Радикал + этанол |
126 |
138 |
1,59 |
220 |
31,1 |
2,66 |
2,66 |
2,16 |
1,54·10-8 |
|
2 |
Радикал + этанол +холестерин |
154 |
103 |
1,47 |
152 |
32,4 |
2,66 |
2,22 |
1,73 |
9,9·10-7 |
|
3 |
Янтарная к-та + хл. + радикал |
187 |
114 |
1,65 |
189 |
31,1 |
2,66 |
2,22 |
2,23 |
1,76·10-8 |
|
4 |
Ацетилсалициловая к-та + хл. + радикал |
31 |
26 |
1,69 |
44 |
31,5 |
1,77 |
2,66 |
1,78 |
1,46·10-8 |
Например, интенсивность системы II НР+ЭТ+ХЛ начало спектра 154 мм, а системы III НР+ЭТ+ХЛ+ЯК и IV НР+ЭТ+ХЛ+АЦК соответственно конец спектра имеют значение 114 мм и 26 мм. Аналогичные изменения наблюдаются в значениях ΔHo, ΔH+1, ΔH-1 – ширина центральной, низкопольной и высокопольной компоненты спектров. Отмечена, разница в параметрах 2A'z – расстояние между низкопольной и высокопольной компонентами спектра и J0/J+1 – отношение интенсивностей высокопольных и низкопольной линий иммобилизованных меток для изученных систем. Как видно из рис. 1 увеличение интенсивности сигнала сопровождается сужением спектральных линии (параметров ΔH+1, ΔH0, ΔH-1). Этот факт объясняется появлением мелкомасштабных движений, приводящих к усреднению дипольных взаимодействий. Эффект сужения (параметров ΔH+1, ΔH0, ΔH-1), по-видимому, связан с движением протонов среди окружающих нитроксильный фрагмент радикала, которые частично усредняют взаимодействие магнитных диполей неспаренного электрона и протона характеризующийся τc ≤ 10-8с.
Спектры ЭПР: а) спиновой метки радикала в этаноле; б) спин-меченного холестерина с радикалом ; в) спин меченного холестерина при погружение в янтарной кислоты; г) спин меченного холестерина при погружение в ацетилсалициловой кислоты при Т = 300 К.
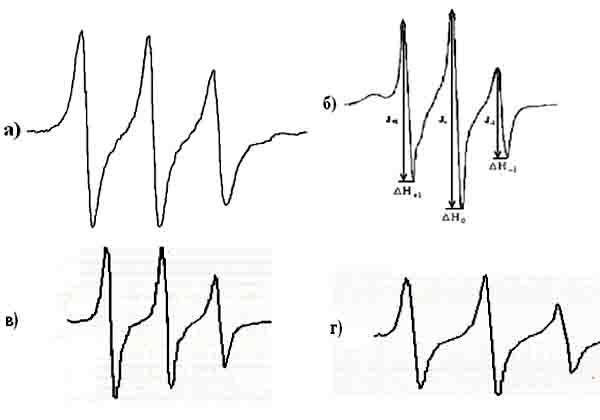
Рис. 1.
В изучении молекулярной структуры биологических объектов методом спиновых меток, одним из достоверных показателей является время корреляции (τc) вращения молекулы. Для наглядности полученные результаты представляем на диаграмме, где отчётливо видна разница в значениях корреляции вращения молекулы в системе 3) НР+ЭТ+ХЛ+ЯК и 4)НР+ЭТ+ХЛ+АЦК по сравнению с системой 1) НР+ЭТ и 2) НР+ЭТ+ХЛ. (см. рис. 2).
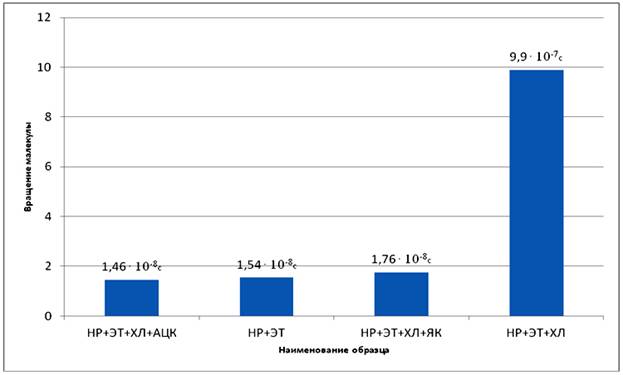
Рис. 2. Диаграмма время корреляции вращения молекулы в системы.
Приведенные данные на диаграмме о времени корреляция «τс» ещё раз указывает о том, что при погружении выше представленных кислот в этаноловый раствор содержащий холестерин, происходит влияние этих кислот на молекулярную структуру холестерина.
Заключение
Таким образом, полученные методом спиновых меток экспериментальные результаты свидетельствуют о том, что янтарная и ацетилсалициловая кислоты в этаноловом растворе содержащий холестерин, влияют на молекулярную структуру холестерина.
Литература
1. Лихтенштейн Г. И. Метод спиновых меток в молекулярной биологии. – М.: Наука, 1974, 256 с.
2. Лихтенштейн Г. И. Многоядерные окислительно-восстановительные ферменты. – М.: Наука, 1979, 323 с.
3. Me Connel H. M., Deal W., Ogata R. T. – Biochemistry, 1969, vol. 8, № 6, р. 2580 – 2585.
4. Кузнецов А. Н. Метод спинового зонда. –М.: Наука, 1976, 210 с.
5. Юсупов И. Х., Бободжонов П. Х., Марупов Р. и др. – Высокомолек. соед., 1984, т. 26А, с. 369 – 373.
6. Бободжанов П. Х., Юсупов И. Х., Марупов Р. - ЖПС, 1992, т.56, № 3, с.
Поступила в редакцию 10.12.2012 г.