Изучение влияния технологических параметров на удельную производительность процесса получения крекинг-газа пиролизом нафты
Медников Евгений Викторович,
кандидат химических наук, доцент,
Щемелинина Ирина Михайловна,
магистрант.
Волгоградский государственный технический университет.
Основными видами сырья для производства полимерных продуктов являются непредельные углеводороды С2-С4, в частности – ацетилен и этилен, значительное количество которых получают различными методами пиролиза углеводородов. В настоящее время основным способом получения олефинов и самого распространенного из них этилена – является пиролиз газообразных и легких жидких углеводородов в трубчатых печах. В настоящее время во всех индустриально развитых странах мира этот способ остается основным.
Синтезы на основе ацетилена, как правило, одностадийные, что способствует снижению образования побочных продуктов и приводит к упрощению технологической схемы. Производство винилхлорида на основе ацетилена дает возможность утилизировать хлористый водород, получающийся как побочный продукт во многих процессах органического синтеза. Ацетилен находит широкое применение в производстве галоидопроизводных и в первую очередь винилхлорида [1, 2]. Большое распространение получил синтез винилхлорида из разбавленной смеси ацетилена и этилена по сбалансированной схеме [1-3].
Пиролиз (термический пиролиз и дегидрирование) углеводородов заключается в разложении и различных превращениях исходных продуктов под действием высоких температур. При этом образуется пиролизный газ, целевыми компонентами которого являются ацетилен и этилен [4].
Процесс позволяет перерабатывать довольно широкий спектр сырья и не нуждается в жесткой привязке к одному поставщику или виду сырья. В качестве сырья для совместного получения ацетилена и этилена теоретически могут быть использованы любые углеводороды и их смеси, газообразные и жидкие. Лучшие результаты получаются при пиролизе парафинов нормального строения, причем, чем длиннее углеродный скелет молекулы, тем процесс более энергетически выгоден.
Практически наилучшими видами сырья являются углеводороды с прямой цепью С3-С7. Использование углеводородов с короткими цепями (метан, этан) энергетически невыгодно, так как требует больших затрат тепла. Применение высокомолекулярных парафинов (свыше С7) приводит к развитию вторичных процессов и увеличенному выходу побочных продуктов и продуктов осмоления.
Технологическая схема пиролиза нафты в потоке газа-теплоносителя с целевым выходом С2Н2 и С2Н4 используется для дальнейшего производства винилхлорида. Винилхлорид получают гидрохлорированием ацетилена [5].
Схема процесса:
Основная реакция на примере бутана: C4H10―>CH2=CH2+CHºCH+2H2.
Побочная реакция: C4H10 ―>2C+H2+2CH4.
Основным процессом является стадия получения этилена и ацетилена из углеводородного сырья, побочная – образование побочных продуктов и продуктов осмоления.
1. Кинетическое уравнения процесса получения крекинг-газа.
Термическое разложение углеводородов представляет собой сложный процесс, который можно представить как ряд протекающих последовательно и параллельно химических реакций с образованием большого числа продуктов. Энергетические характеристики реакций, определяют направления и максимальную равновесную степень превращения по ним исходных веществ. Равновесную степень превращения по химической реакции можно вычислить из уравнения зависимости энергии Гиббса (свободной энергии, G°):
![]() (1)
(1)
Изменение стандартной энергии Гиббса определяется разностью стандартных значений энергии Гиббса образования конечных и исходных веществ реакции. Степень превращения χ исходных веществ по реакции является однозначной функцией константы равновесия Kp , аналитическое выражение которой определяется стехиометрией реакции.
Уравнение скорости реакции получения крекинг-газа:
r=k*P0 бутана (2)
Превращение бутана описывается реакцией первого порядка и для константы скорости этой реакции получено выражение:
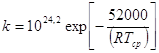 (3)
(3)
Из уравнения Арениуса:
Для основной реакции: k1= 1024,2exp[-52000/RTср]; (4)
Для побочной реакции: k2= 1023,2exp[-34000/RTср] [6] (5)
2. Влияние технологических параметров на удельную производительность рив.
2.1. Влияние конверсии бутана на удельную производительность.
Удельная производительность – характеристика реактора, которая показывает какое количество целевого продукта образуется в единице реакторного объема в единицу времени.
Для реактора РИВ удельную производительность вычисляют по уравнению:
![]() , (6)
, (6)
где FB – мольный расход целевого продукта (В); VРИВ – реакционный объем; FA,0 – мольный начальный расход реагента А; XA – конверсия реагента А; ФВ – селективность основной реакции по целевому продукту (В).
График зависимости удельной производительности реактора от конверсии бутана представлен на рис. 1.
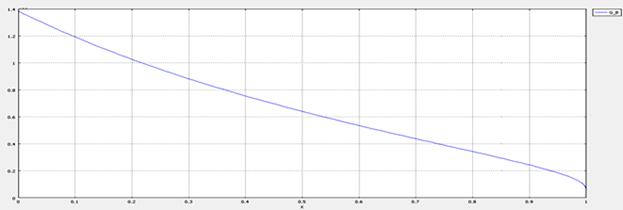
Рис. 1. График зависимости удельной производительности РИВ от конверсии бутана.
С увеличением конверсии реагента уменьшается его количество, а следовательно, замедляется скорость реакции. Поскольку удельная производительность пропорциональна скорости реакции, то с замедлением реакции уменьшается значение УП. Этим объясняется убывающий характер кривой G=f(Х).
2.2. Влияние парциального давления бутана на удельную производительность.
График зависимости удельной производительности РИВ от парциального давления реагента А представлен на рис. 2.
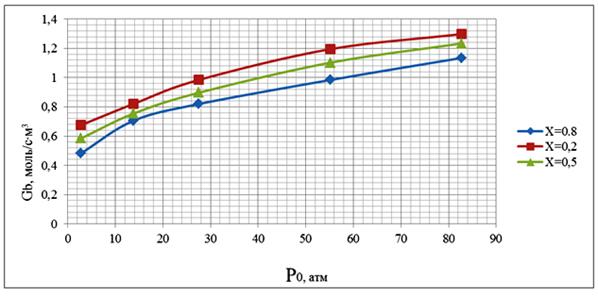
Рис. 2. График зависимостей удельной производительности РИВ от парциального давления бутана.
Линейный характер кривой Gb=f(F0) объясняется тем, что скорость реакции образования крекинг-газа описывается уравнением: r=k*Pб.
Из уравнения видно, что чем больше значение парциального давления бутана, тем больше скорость реакции, следовательно, и удельная производительность реактора.
1. Паушкин Я.М. Нефтехимический синтез в промышленности. – М.: Наука, 1996 г.
2. Антонов В.Н., Лапидус А.С. Производство ацетилена. – М.: Химия, 1990 г.
3. Braconier F. Haw SBA makes vinil chloridehydrocorbon. Process and Petrol. Refiner. 1994, №11.
4. Лебедев Н.Н. Химия и технология основного органического синтеза. – М: КолосС, 2013 г.
5. Основной технологический регламент цеха № 102 ОАО «Каустик». Волгоград, 2008.
6. Мухина Т.Н., Баранов Н.Л., Бабаш С.Е. и др. Пиролиз углеводородного сырья.1987 г.-240 стр.
Поступила в редакцию 12.05.2014 г.