О проблеме биодеструкции некоторых ксенобиотиков
Белов Денис Владимирович,
кандидат химических наук, доцент кафедры фармацевтической химии и фармакогнозии Нижегородской государственной медицинской академии.
Катализируемые ферментами реакции посторонних для окружающей среды веществ, т.е. чужеродных органических соединений (ксенобиотиков), можно считать желательными или нежелательными в зависимости от того, какие продукты при этом образуются. Желательными можно считать вещества с малой токсичностью (при этом будет происходить их детоксикация), соответственно для органических веществ – полное разложение или возвращение в природную систему обмена веществ. Нежелательные конечные или промежуточные продукты биотических реакций имеют повышенную активность по отношению к экосистемам и человеку.
При ферментативном воздействии микроорганизмов на органические вещества возможны как минимум два процесса. В первом случае органическое вещество разлагается до неорганических продуктов, таких как диоксид углерода, хлориды и т. п., или до низкомолекулярных органических фрагментов, способных участвовать в природных циклах углерода. Такие превращения сопровождаются приростом биомассы соответствующих организмов, что указывает на то, что они получают в этих реакциях углерод и энергию для биосинтеза (метаболизм). Однако такого рода биологические превращения возможны лишь для небольшого числа химических соединений и живых организмов, прежде всего – для микроорганизмов почвы, воды или донного ила. Большинство химических соединений превращаются микроорганизмами по второму пути, называемому кометаболизмом. С его помощью организмы преобразуют ксенобиотические соединения, не получая из них ни углерода, ни энергии, т.е. этот процесс не обеспечивает их роста. Образованные из ксенобиотических веществ продукты также являются химическими веществами, посторонними для окружающей среды, т.е. их также следует рассматривать как антропогенные вещества.
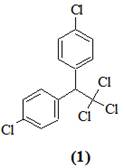
Одной из наиболее сложных задач, стоящих перед обществом в связи с необходимостью защиты биосферы от токсических веществ, является разработка методов рационального применения пестицидов. Основным принципом, определяющим перспективу исследований в этой области, следует считать создание пестицидов, остатки которых быстро разлагаются в биосфере естественным путем без образования интермедиатов, обладающих токсическим, канцерогенным или мутагенным действием. Однако реальная ситуация в настоящий момент может осложняться тем, что в биосфере уже накопилось некоторое количество остатков очень стойких пестицидов или продуктов их превращения. Поступление этих соединений в почву, водоемы, атмосферу продолжается, так как современное сельское хозяйство немыслимо без пестицидов, несмотря на то, что имеющиеся сейчас в нашем распоряжении препараты не удовлетворяют сформулированным выше требованиям. Следовательно, проблема освобождения биосферы от остатков стойких пестицидов остается, и долгое время еще будет оставаться весьма актуальной. В частности, до сих пор не снят вопрос о необходимости освобождения биосферы от пестицида с тривиальным названием ДДТ – 1,1,1-трихлор-2,2-бис-(n-хлорфенил)-этана (1) [1].
Деградация ДДТ культурой бактерии Pseudomonas sp. 640x.
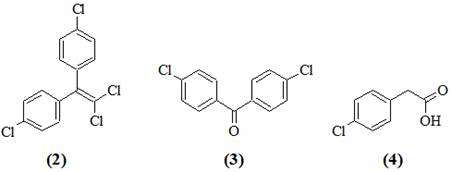
Поиск наиболее рациональных путей биоразложения ксенобиотиков, таких как ДДТ, очень сложная комплексная задача. Основные усилия направлены на получение культур микроорганизмов, способных разлагать ДДТ до нетоксических продуктов. Установлено, что некоторые микроорганизмы способны трансформировать ДДТ (1) до 1,1-дихлор-2,2-бис-(n-хлорфенил)-этилен (ДДЕ) (2) и n,n-дихлорбензофенон (ДБФ) (3) [1]. При этом происходит частичное дехлорирование молекулы, но продукты трансформации по своей потенциальной опасности для биосферы мало отличаются от ДДТ. Наиболее глубокое расщепление ДДТ достигнуто с помощью культуры Pseudomonas sp., выращенной на питательной среде, содержащей дифенилметан [2], которая в условиях двухстадийной ферментации превращала ДДТ в n-хлорфенилуксусную кислоту (4).
Целью исследований [1] был поиск культур микроорганизмов, способных разлагать ДДТ до конечных продуктов или до нехлорированных соединений, являющихся обычными микробными метаболитами.
Работа проводилась путем высевов культур микроорганизмов из садовых почв, длительное время обрабатывающихся ДДТ, на питательные среды с дополнительными питательными субстратами. Детально была изучена деградация ДДТ культурой Pseudomonas sp. 640x. Хроматомасс-спектрометрический анализ продуктов деградации ДДТ показал наличие трансформации в присутствии различных дополнительных субстратов. На среде с октаном, гексаном, бутиратом и глюкозой среди продуктов деградации были обнаружены ДДЕ (2) и бис-(4-хлорфенил)уксусная кислота (5). Значительно более глубокое разложение ДДТ наблюдали на среде с гексадеканом. Через месяц культивирования в среде накапливался n,n-дихлорбензгидрол и n,n-дихлордифенилметан, к концу второго месяца культивирования среди продуктов деградации преобладала фенилуксусная кислота (6).
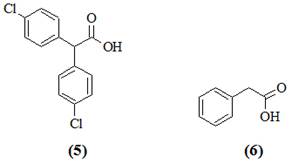
Таким образом, культура Pseudomonas sp. 640x осуществляет полное дехлорирование ДДТ и расщепление одного из ароматических циклов молекулы с образованием фенилуксусной кислоты (6), которая не метаболизируется данной культурой, но является веществом, легко доступным для многих микроорганизмов. При исходной концентрации ДДТ 50 мг/л через 2 мес. 50 % пестицида превращалось в фенилуксусную кислоту (6), 10 % трансформировалось в ДДЕ (2) и 40 % оставалось интактным.
Периферийный метаболизм ароматических углеводородов у микроорганизмов часто сопровождается накоплением в среде продукта их частичного превращения. Во многих случаях эти продукты являются интермедиатами процесса использования углеводородов как источников углерода и энергии. Например, было обнаружено накопление в среде диметилбензойных кислот при росте Pseudomonas aeruginosa 7 на псевдокумоле (1,2,4-триметилбензоле) [3]. Наряду с этим известны многочисленные примеры, когда продукты частичного превращения накапливаются в среде без дальнейшего использования их культурой. Такие процессы представляют собой типичные микробиологические трансформации.
Микробиологическое окисление мезитилена.
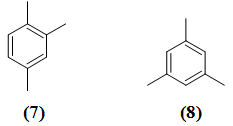
При изучении окисления ароматических углеводородов псевдомонадами было обнаружено, что штамм Pseudomonas aeruginosa 7 активно рос на псевдокумоле (1,2,4-триметилбензоле) (7), но мезитилен (1,3,5-триметилбензол) (8) не поддерживал роста культуры [4]. Из литературных данных известно, что мезитилен не окисляется микроорганизмами. В работе [4] описывается изучение окисления мезитилена штаммом Pseudomonas aeruginosa 7, способным использовать этот углеводород в качестве ростового субстрата.
Микробное гидроксилирование ароматических и гетероароматических соединений активируется соответствующими ферментными системами с участием молекулярного кислорода и воды. Так, при биодеградации соединений ряда бензола первоначальное образование гидроксилированных продуктов осуществляется соответствующими гидроксилазами с использованием молекулярного кислорода [5, 6]. В случае ароматических соединений пиридинового ряда, таких, как никотиновая и пиколиновая кислоты, оксипиридин, происходит активируемое гидроксилазами включение OH-группы с использованием кислорода воды [7–9].

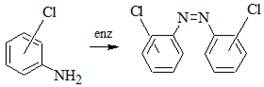
Галогензамещенные анилины накапливаются в почве в процессе трансформации целого ряда анилинсодержащих пестицидов, поэтому их дальнейший метаболизм микроорганизмами представляет большой интерес. Наиболее хорошо изучены процессы конденсации галогензамещенных анилинов под действием почвенных микроорганизмов, в основном микроскопических грибов, обладающих пероксидазной активностью, в результате которых образуются симметричные и несимметричные азобензолы [10]. Однако такой путь метаболизма галогензамещенных анилинов не является основным при их трансформации в почве, так как азобензолы обнаруживались лишь в незначительных концентрациях и не во всех почвах [11].
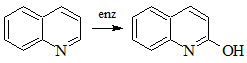
Гидроксилирование хинолина бактериями Pseudomonas aeruginosa.
Было показано [12], что бактерии Pseudomonas aeruginosa при росте на питательной среде, содержащей хинолин, образуют 2-оксихинолин. Полученный продукт бактериального окисления хинолина образуется как с участием кислорода воды, так и молекулярного кислорода. Высказано предположение [13], что кислород гидроксильной группы 2-оксихинолина первоначально образуется за счет включения молекулярного кислорода, а затем происходит обмен его с водой. В отличие от ароматических и полициклических соединений в реакции гидроксилирования хинолина, осуществляемой бактериями Pseudomonas aeruginosa Р1, участвует гидроксильная группа воды.
Ацетилирование культурой Pseudomonas aurantiaca анилина и его хлорзамещенных аналогов.
Изучен другой путь микробиологической трансформации анилинов – образование ациланилидов. Показано, что 4-броманилин ацетилируется почвенными микроорганизмами, 4-хлорацетанилид является одним из промежуточных продуктов окисления 4-хлоранилина микроскопическим грибом Fusarium oxysporum; ацетилированный метаболит был обнаружен также при изучении трансформации фунгицида 2,6-дихлор-4-нитроанилина в почве [14].
В работе [14] приводятся доказательства того, что основными продуктами трансформации анилина (10) и его 3-хлор- (11), 4-хлор- (12) и 3,4-дихлор-замещенных аналогов (13) под действием бактерии Pseudomonas aurantiaca № 1 в соокисленных условиях могут являться соответствующие хлорированные ацетанилиды.
Выход ацетилированных продуктов при оптимальных условиях колеблется от 30 до 80 % в зависимости от субстрата трансформации.
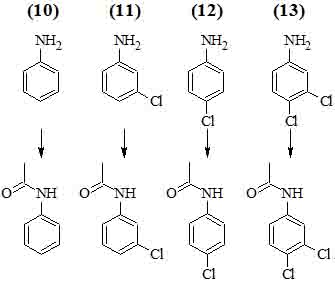
Бактерия Pseudomonas aurantiaca № 1 была выделена из почв кубанских рисовых полей, в течение ряда лет обрабатываемых пестицидом – пропанидом (3,4-дихлорпропиоанилид или N-(3,4-дихлорфенил)пропионамид) (14):
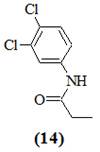
Установлено, что Pseudomonas aurantiaca № 1 трансформирует анилин (10) и его хлорированные аналоги (11)–(13). Скорость и полнота трансформации зависят как от субстрата, так и от концентрации глюкозы в питательной среде. Полученные экспериментальные данные свидетельствуют о том, что ацетилирование является основным путем трансформации анилинов бактерией Pseudomonas aurantiaca № 1. Ацетилированные продукты не были обнаружены лишь в случае 2-хлоранилина. Роль глюкозы как косубстрата в данном случае сводится, по-видимому, к созданию пула ацетильных групп, необходимых для трансформации анилинов.
В отличие от микроскопических грибов Fusarium oxysporum и Geotrichum candidum, для которых характерна трансформация хлорированных анилинов путем окисления аминогруппы, приводящая к образованию азобензолов, выделенный из почвы штамм бактерии Pseudomonas aurantiaca № 1 трансформирует хлорированные анилины в условиях кометаболизма в менее токсичные ацетанилиды.
Результаты работы [14] позволяют сделать вывод о возможности протекания в почве процессов микробиологической трансформации анилинсодержащих пестицидов, не связанных с образованием азобензолов, обладающих токсическим и канцерогенным действием по отношению к животным.
В комплексе проблем, связанных с загрязнением Мирового океана, наряду с глобальным распространением в морской среде нефтяных углеводородов, привлекающим пристальное внимание мировой научной общественности, в последнее время приобретает приоритетное значение проблема ксенобиотиков, к которым относятся, в частности, полихлорированные бифенилы (ПХБ).
Микробная трансформация полихлорированных бифенилов в полярных морских регионах.
Загрязнение морей полихлорированными бифенилами (ПХБ) (15) имеет ряд специфических особенностей.
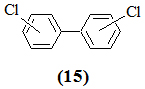
Во-первых, ПХБ довольно устойчивы к химическому разложению, что способствует их накоплению в различных объектах морской среды в биоцидных дозах (в промысловых организмах – в дозах, токсичных даже для здоровья людей); во-вторых, для них характерен непрямой мутагенный эффект [15]; в-третьих, в настоящее время доказано, что загрязнение полихлорированными углеводородами природной среды имеет глобальный характер, объясняемый дальними переносами их через атмосферу и гидросферу, а Мировой океан играет роль “конечного резервуара” для этих химических соединений [16, 17].
В работе [18] сообщалось о распространении в разных районах Мирового океана и микробной трансформации в морской воде полиароматических углеводородов на примере бенз[а]пирена.
Известно, что микроорганизмы исключительно быстро адаптируются к появлению новых экологических факторов природного и антропогенного характера. Известно, что в основе адаптации микроорганизмов к новым источникам питания лежит появление новых функционально активных ферментов (например, многоцелевых оксидаз), связанное с изменением генофонда бактерий, в частности, за счет плазмид [19].
Работа [19] посвящена изучению способности морской микрофлоры трансформировать полихлорированные бифенилы в полярных регионах Мирового океана. Было установлено широкое распространение ПХБ в разных объектах экосистем Берингова и Чукотского морей. Одновременно изучалась микрофлора, способная трансформировать ПХБ. Концентрация микрофлоры составляла до нескольких сотен клеток в 1 мл воды. Уровни разрушения, например, пентахлорбифенилов оказались близкими между собой и колебались в пределах 36 – 44 %.
Анализ когерентов ПХБ, подвергавшихся микробной деградации, показал, что на процессы деструкции смесей ПХБ в первую очередь влияют стерические особенности молекул и только затем число галоидных атомов-заместителей. Исследованиями показано, что в полярных районах океана активной бактериальной деградации подвергаются только низкохлорированные (ди- … гексахлор-)бифенилы. Однако многие из этих соединений разрушаются лишь частично, либо трансформируются в другие вещества, которые могут быть также опасны для морской биоты. Что касается высокохлорированных бифенилов, то они обладают высокой устойчивостью к воздействию морских микроорганизмов, аккумулируются в компонентах экосистем и циркулируют в морской среде в течение многих десятилетий.
Результаты работ свидетельствуют о большой экологической опасности загрязнения хлорированными углеводородами полярных районов Мирового океана, где в условиях низких температур микробная трансформация ксенобиотиков протекает медленно, а процессы химического разрушения практически не происходит.
Среди анионных поверхностно-активных веществ (АПАВ) алкилбензолсульфонаты (АБС) – одни из наиболее устойчивых к микробному разложению. Тем не менее, из экономических соображений они широко применяются в качестве компонентов синтетических моющих средств (СМС), представляя, таким образом, серьезную угрозу загрязнения воды. Известно, что некоторые микроорганизмы способны осуществлять деструкцию АБС [20]. В работе [21] предложен микробиологический метод очистки от АПАВ промышленных сточных вод. Метод основан на использовании специально селекционированных высокоактивных микробов-деструкторов. В работе [22] описан способ выделения штамма бактерий, способного разрушать АБС, и изучение закономерностей бактериальной деструкции этих веществ.
Бактериальная деструкция алкилбензолсульфонатов.
При производстве синтетических моющих средств (СМС) применяется технический препарат АБС – хлорный сульфонол, характеризующийся сравнительно низкой биоразлагаемостью из-за высокого содержания разветвленных цепей.
CnH2n+1C6H4SO3Na (CnH2n+1)( CmH2m+1)CHSO3Na
Бактерии выращивали на среде, содержащей сульфонол. Изучена способность коллекционных бактерий (всего 106 штаммов) родов Pseudomonas, Escherichia, Enterobacter, Flavobacterium, Achromobacter, Proteus, Bacillus, Micrococcus, Staphylococcus, Sarcina, Arthrobacter, Nocardia использовать изучаемые образцы АБС в качестве единственного источника углерода, серы и энергии. Среди этих культур 38 являлись деструкторами различных ксенобиотиков: нитросоединений, красителей, морфолина, диэтиленгликоля, анионных, амфолитных и неионогенных ПАВ. Показано, что практически все исследованные штаммы не растут на среде с АБС. Культура накопления, обладающая такой способностью, получена путем длительной обработки раствором сульфонола в условиях протока почвы, отобранной на территории завода по производству СМС. При пассировании на питательной среде это свойство утрачивалось. Полученной накопительной культурой заселяли лабораторный биореактор. Спустя несколько месяцев в биореакторе была достигнута удовлетворительная степень очистки подаваемой загрязненной АБС жидкости.
Исследование микроорганизмов, выделенных из биореактора, показало явное доминирование одного бактериального штамма, который был изолирован и идентифицирован как Pseudomonas alcaligenes TR. Полученный штамм в условиях периодического культивирования разрушал прямоцепочечный АБС и практически не использовал разветвленный. Гомологи АБС с четным числом атомов углерода в цепи разрушаются быстрее и более полно, чем вещества с нечетным количеством атомов. Эффективность деструкции повышается также при увеличении длины углеводородного радикала. Исследуемый штамм бактерии разрушал и другие ПАВ: первичные и вторичные алкилсульфонаты, динатриевую соль моноалкилсульфоянтарной кислоты, алкилметилтаурин (метаупон), циклимид, амидобетаин.
В качестве промежуточных продуктов деструкции АБС штаммом Pseudomonas alcaligenes TR идентифицированы алкилбензолы и жирные кислоты. После продолжительного культивирования бактерий наблюдается полное исчезновение соединений бензольного ряда.
Штамм Pseudomonas alcaligenes TR апробирован в условиях опытно-промышленной проверки микробиологического метода очистки от сульфонола ливневых и технологических сточных вод завода бытовой химии [22]. Полученные результаты позволяют использовать изученный штамм при очистке многокомпонентных промышленных сточных вод, содержащих наряду с АБС, другие ПАВ.
Заключение
Для новых соединений, которые постоянно поступают в окружающую среду (по аналогии с рассмотренными выше примерами), при сравнении их структуры с уже исследованными посторонними веществами можно сделать некоторые прогнозы об их биологической устойчивости.
Проблема борьбы с загрязнением окружающей среды ксенобиотиками все более остро осложняется тем, что почвенная или водная микрофлора не способна к переработке столь большого количества поступающих в экосистемы веществ, и аккумулирующихся в них. Постепенное возрастание предельно допустимых концентраций по каждому из компонентов неизбежно ведет к синергетическому эффекту, т.е. пагубное воздействие одних веществ усиливается ввиду присутствия в системе других. Локальное концентрирование в среде ксенобиотиков создает предпосылки к полному уничтожению любых видов микрофлоры, что способствует дальнейшему аккумулированию этих соединений и возникновению повторных и более сильных синергетических эффектов. Если микробиота не успевает модифицировать или полностью уничтожить ксенобиотические вещества, или что еще губительнее – становится неспособной это делать, она погибнет. Очевидно, что в условиях отсутствия микрофлоры в экосистемах, и сами экосистемы прекратят свое существование. Ксенобиотики – это бомба замедленного действия. С возникновением и распространением новых органических или вновь синтезированных и внедренных в повседневное применение веществ, создается предпосылка к их аккумулированию в экосистемах окружающей среды. Микроорганизмы могут попросту не успеть разложить или модифицировать все те вредные вещества, которые в таком огромном количестве поступают в окружающую среду. Неизбежно это приведет к пагубным последствиям для всего живого на планете.
Литература
1. Скрябин Г.К., Головлева Л.А., и др. – ДАН, 1977, т. 237, № 5, с. 1212 – 1215.
2. Pfaender F.K., Alexander M. ibid., 1972, v. 20, p. 848.
3. Головлева Л.А., Червин И.Н. и др. – ДАН, 1975, т. 222, № 6, с. 1448.
4. Головлева Л.А., Ганбаров Х.Г., и др. – ДАН, 1977, т. 234, № 3, с. 706 – 708.
5. Jibson D.T., Cardini G.E., Masels G.C., Kellio R.E. – Biochemistry, 1970, vol. 9, p. 1631 – 1635.
6. Yamaguchi M., Yamagychi T., Fujisava H. – Biochem. Biophys. Res. Comm., 1975, vol. 67, p. 264 – 271.
7. Kunt A.L., Hughes D.E., Lewenstein J.M. – Biochem. J., 1958, vol. 69, p. 170 – 173.
8. Ewens W.C. – Biochem. J., 1967, vol. 103, p. 1 – 5.
9. Hougton C., Cain R.B. – Biochem. J., 1972, vol. 130, p. 879 – 893.
10. Bollaf J.M. Adv. – In Appl. Microbiol., 1974, v. 18, p. 75.
11. Соколов М.С., Кныр Л.И. и др. – Химия в с. х., 1975, т.3, с. 64.
12. Дзумедзей Н.В., Шевченко А.Г., и др. – Микробиология, 1983, т. 52, № 2, с. 209 – 212.
13. Шевченко А.Г., Старовойтов И.И., и др. – ДАН, 1990, т. 310, № 6, с. 1493 – 1495.
14. Суровцева Э.Г., Васильева Г.К., и др. – ДАН, 1977, т. 237, № 1, с. 220 – 223.
15. Цыбань А.В. Экологический мониторинг Балтийского моря. М.: Гидрометеоиздат, 1983. 15 с.
16. Израэль Ю.А., Цыбань А.В., Панов Г.В. и др. Всесторонний анализ окружающей природной среды. Тр. V Советско-американского симпозиума. Л.: Гидрометеоиздат., 1988, с. 77 – 111.
17. Tanabe S. – J. Oceanogr. Soc. Japan, 1982, vol. 38, p. 137 – 148.
18. Цыбань А.В., Шабад Л.М., Хесина А.Я. и др. – ДАН, 1980, т. 252, № 6, с. 1490 – 1493.
19. Израэль Ю.А., Цыбань А.В., Панов Г.В. и др. – ДАН, 1990, т. 310, № 2, с. 502 – 506.
20. Bird J.A., Cain R.B. – Biochem. J., 1974, vol. 140, № 2, p. 121 – 134.
21. Ставская С.С. и др. – Хим. и технол. воды, 1982, т. 4, № 4, с. 368 – 370.
22. Ротмистров М.Н., Таранова Л.А., Радченко О.С. и др. – ДАН, 1986, т. 288, № 1, с. 246 – 248.
Поступила в редакцию 20.04.17 г.